Ni som följt min blogg ett tag vet att jag har skrivit om det här förr. Under förra julen (2012) och även in i januari förra året så skrev jag en serie poster kring hur alkohol kokas bort ur vinsås och annan mat.
Dessa poster försvann i flytten av bloggen och ärligt talat var de också både onödigt babbliga och svårtillgängliga. Jag har fått anledning att tänka på det här igen och då tänker jag passa på att gå igenom lite grundläggande fysikalisk kemi och prata om både vinsåser (och hembränd sprit). Poängen med den här posten är att ta fram några verktyg för hur man ska kunna göra alkoholfri mat. Hur mycket ska maten koka innan man kan betrakta den som alkoholfri?
Jag är född och uppvuxen i Hälsingland, vilket gör att jag i princip har hembränningen i blodet så de här frågorna faller väldigt naturligt för mig. Som alla bollnäsbor så lärde jag mig i tidig ålder att sprit kokar vid 78,5 °C. Vad en hembrännare ska med den kunskapen till är väldigt oklart då den där kokpunkten bara gäller ren alkohol. Jag kommer tillbaka till det nedan.
Nåja, innan jag kör igång den här monsterposten så vill jag bara inflika några viktiga saker. Jag kommer prata om både etanol och alkohol i fortsättningen och kanske använda begreppen lite slarvigt, men jag menar alltid etanol. Alkohol är ett samlingsnamn för en stor mängd olika substanser och det är just etanolen som är den intressanta i det här fallet. För mig som kemist så kommer ordet etanol väldigt naturligt och därför kommer det nog vara lättast att skriva för mig när det blir väldigt kemiskt. Det här kan också bli ett väldigt teoretiskt inlägg och kanske t o m lite svårt. Man bör kunna följa resonemanget oavsett utbildning och i alla fall slutklämmen kan alla alla utnyttja, utan att kanske riktigt förstå varför det är så. Jag kommer börja med lite grundläggande kemi och fysik för att sedan bli mer specifik.
Etanol i mat
Vi använder vin, sprit och diverse andra alkoholprodukter i matlagningen och de flesta tycker nog också att vinet verkligen höjer smaken. En vällagad rödvinssås, en svampsoppa med sherry eller en marmelad med rom – rätterna höjs liksom ett snäpp genom tillsatsen av något alkoholhaltigt.
Av olika skäl kan den där skvätten rödvin i såsen oroa människor. Det kanske är så att man inte vill ge sina barn något som innehåller alkohol eller kanske är det en gravid kvinna som är försiktig. Man kan också ha religiösa skäl. Innan jag går djupare in på alkoholhalter i kokade såser så vill jag bara påpeka att en helt okokt rödvinssås (så gör man inte rödvinssås), som innehåller 50:50 rödvin och buljong, har en alkoholhalt på runt 7%. Till en portion tar du i värsta fall en halv deciliter (då badar verkligen maten i sås) och då får du i dig 3,5 ml ren etanol. En lättöl innehåller ungefär den dubbla mängden etanol. Så det borde vara en icke-fråga för den gravida kvinnan och den oroliga föräldern men jag tänker inte döma någon för varandes försiktig. Låt oss behandla frågan akademiskt och reda ut den ändå, annars har ju inte jag något att blogga om heller.
Kokpunkten
Kokpunkten för en vätska är den temperaturen då ångtrycket hos vätskan är lika stort som det omgivande trycket och således temperaturen då vätskan övergår till gas. En vätska kan också förångas i temperaturer under kokpunkten men det sker då bara vid ytan. Bubblorna när en vätska kokar är bubblor av vätskan i gasform som bildas i bottnen av kärlet och sedan färdas uppåt. Bubblorna i det kokande vattnet är alltså fyllda med enbart vatten i gasform. Inte att förväxla med ånga egentligen då ånga är små droppar som syns från t ex skorstenen hos ett ånglok. Vatten i gasform sprider varken ljus eller har någon färg så den syns inte.
Vid kokpunkten är alltså trycket utåt från vätskan lika stort som det omgivande lufttrycket. Det betyder att kokpunkten beror av lufttrycket och befinner du dig uppe på ett högt berg så kommer lufttrycket vara lägre och således behöver du inte hetta upp vätskan lika mycket för att dess ångtryck ska bli lika högt om lufttrycket. Vatten kokar vid ungefär 70 °C längst upp på Mount Everest. I fortsättningen kommer vi tala om förhållanden med normalt lufttryck, alltså trycket som föreligger vid havsytan.
Hur fort vätskan övergår i gasform under kokning beror inte av temperaturen på det som kokar. Kokar vatten så är det 100 °C, oavsett om det bara puttrar lite eller stormkokar. Stormkokning innebär att det går lite fortare bara och att man väldigt lokalt i materialet i bottnen av kastrullen ligger lite högre i temperatur. Återigen gäller det här normaltryck, i t ex en tryckkokare kan vatten komma upp i högre temperaturer. En annan sak som påverkar hur fort det här går är hur stor yta du har på det du kokar. Du kokar garanterat snabbare bort en liter vatten i en traktörpannan än i en smal och hög kastrull. Ytterligare något som påverkar hur fort en vätska kokar bort (menar alltså egentligen övergår i gasform) är hur bra gasen transporteras bort. Det finns liksom bara plats för en viss mängd gasmolekyler alldeles ovanför ytan och för att mer ska få plats måste det hela tiden ske en transport av gas bort från ytan. Har du en bra köksfläkt så reducerar du snabbare ner din portvinssky. Det här vet alla egentligen intuitivt, det är av exakt samma skäl som blöt tvätt torkar snabbare när det blåser ute.
Kokpunkten för etanol-vatten-blandningar
Vi har talat om vad kokpunkten är så nu kan vi bli mer specifika. Vatten och etanol är fullståndigt lösliga i varandra, vilket innebär att de blandas fullständigt och blandningens fysikaliska egenskaper blir gemensamma egenskaper. D v s blandningen får en gemensam fryspunkt, en gemensam kokpunkt, ett gemensamt ångtryck och en gemensam densitet med mera. En gemensam kokpunkt alltså… Det är inte så att om du kokar finkonjaken så kommer vätskan först börja koka vid 78 °C och där koka bort etanolen och sedan sticka iväg till 100 °C och där koka bort vattnet. Nej, kokpunkten är gemensam och beror av blandningens sammansättning. I Fig 1 visas ett diagram över hur kokpunkten varierar med etanolinnehållet i en etanol-vatten-blandning.
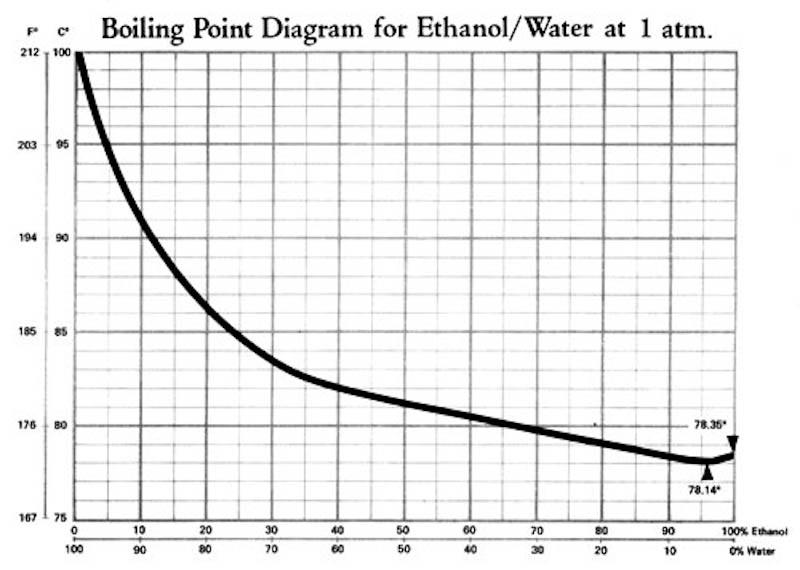
Fig 1. Kokpunkten hos etanollösningar
Där ser vi t ex att finkonjaken (40%) kokar vid drygt 80 °C, glöggen (15%) kokar vid 90 °C och stroh-romen (80%) som Freddie snodde av sin morsa i åttan kokar vid 75-80 °C. Det här kan du testa om du inte litar på mig. Vanliga hushållstermometrar är ofta väldigt pålitliga i intervallet 0-100 °C och det är bara att du kokar upp skitvinet, stoppar ner en termometer och läser av. OBS. Det är vikt-% i Fig 1, använd Fig 2 om du vill testa.
Sammansättningen hos vätskefasen och gasfasen
Det man måste fråga sig är vad det är som övergår från vätskefas till gasfas när din etanollösning (alla alkoholdrycker och mat med alkohol i är etanollösningar) kokar. Om du kokar konjaken, har då också gasen ett etanolinnehåll på 40%? Nej, det har den inte. Gasen innehåller proportionellt mer etanol än vätskan vid en viss temperatur. Detta går att läsa ut ur Fig 2, där gasens sammansättning vid olika temperaturer representeras av den röda kurvan. Den blå kurvan är samma som är utritad i Fig 1. Nu inser jag att det kan bli lite svårt och jag tänker inte förklara varför den röda kurvan ser ut som den gör, vill ni förstå den så läs universitetskemi.
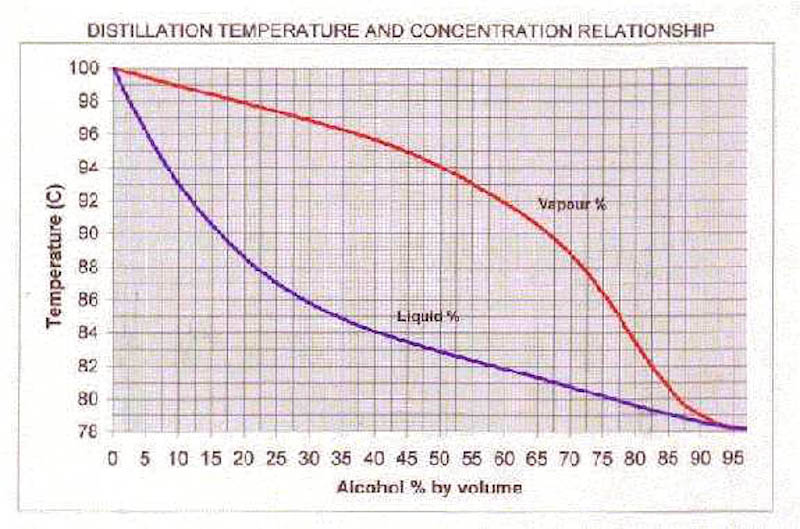
Fig 2. Fasdiagram etanol-vatten
Det här med att gasen innehåller procentuellt mer etanol än vad vätskan gör vid kokpunkten är nyckeln till destillering. Vid destillering kyls gasen så den kondenserar (övergår från gas till flytande) och får rinna ner i ett annat kärl. Man kan ta reda på vad sammansättningen är på gasen genom att dra några linjer i Fig 2. Det har jag gjort och det blir nu Fig 3.
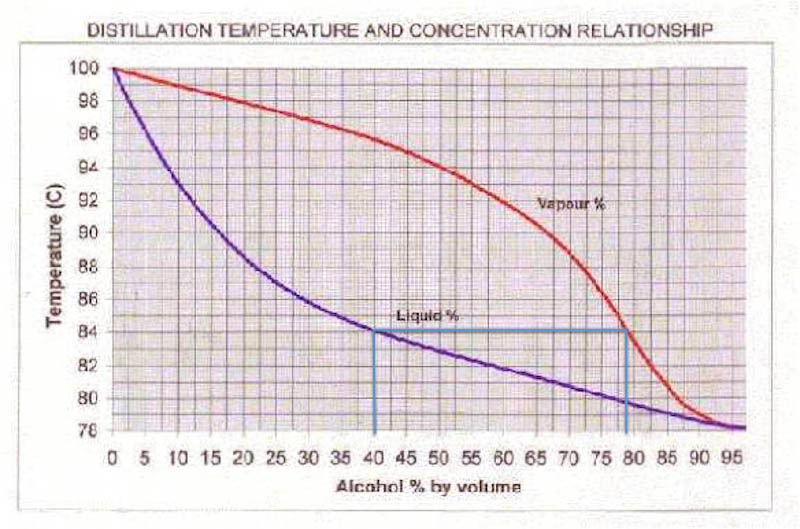
Fig 3.
Låt oss använda Fig 3 och ta reda på vad den bildade gasen har för alkoholhalt när vi kokar finkonjaken. Dra en linje upp till den blå kurvan från x-axeln (horisontella axeln i diagrammet). Där kan vi läsa av kokpunkten som 84 °C. Observera att det är lite fel det som står under Fig 1, där har jag utgått från vikt-%. Här är det dock rätt.
Dra sedan en horisontell linje åt höger tills du stöter på den röda kurvan. Dra sedan ner och läs av sammansättningen. Det är sammansättningen på den bildade gasen. Kokar du konjaken så har den bildade gasen en alkoholhalt på ungefär 77 %. Det är så klart bara när den precis börjar koka. Under tiden som mer gas sticker iväg så sjunker ju givetvis alkoholhalten i vätskan. Ha! Precis vad vi är ute efter när det kommer till rödvinssåsen.
Hur sjunker alkoholhalten under kokning?
Här börjar det bli riktigt knepigt. När jag tänkte på det här första gången, för lite drygt ett år sedan, så insåg jag att man borde kunna räkna på det som sker. Man borde kunna korrelera volymsminskningen på vätskan mot alkoholhalten i den. Dessvärre är jag ingen vidare fena på matte så jag efterlyste hjälp här på bloggen. Hjälp fick jag också av en civilingenjör vid namn Henrik Gustavsson. Han gjorde ett simuleringsprogram i Excel som kan användas för att simulera hur alkoholhalten sjunker med volymenreduktionen med hjälp av differentialkalkyl. I programmet kan jag mata in ursprungskoncentrationer och få ut hur mycket jag ska reducera den för att erhålla en alkoholhalt som är 0,5% (det är definitionen av alkoholfritt). Är du intresserad av det kalkylbladet så släng iväg ett mail till mig så skickar jag det.
Man ska komma ihåg att det har gjorts en del approximationer här. Salter och sockerarter, som så klart finns i mat, ändrar kokpunkten hos en vätska. Dock har jag antagit att de förekommer i så små mängder så det inte påverkar kokpunkterna nämnvärt.
Snabbtest av alkoholhalt i såsen
Utifrån ovanstående resonemang kommer i alla fall en snabb metod för att mäta alkoholhalten på vinsåsen – mät helt enkelt kokpunkten. Stoppa ner en termometer när såsen kokar och läs av. Ligger temperaturen nära 100 °C så är såsen (eller grytan) i princip alkoholfri. Så enkelt är det faktiskt. Metoden är släkt med sättet som en alkoholmätare för hemmagjort vin funkar. Där utnyttjar man istället att alkoholen påverkar densiteten hos vätskan och densiteten kan sedan omvandlas till en alkoholhalt.
Den här metoden stämmer tillräckligt bra. I alla fall bättre än många publicerade knäppmetoder som beskriver hur lång tid det tar att koka ur alkoholen. Tiden beror alldeles för mycket på yttre omständigheter (kärlform, köksfläktens funktion mm) för att vara en pålitlig indikator.
Ber om ursäkt för onödigt nörderi kring ett icke-problem men jag ville ha det här nedskrivet någonstans. När jag googlade på det här för lite drygt ett år sedan så insåg jag att nog ingen tacklat det här problemet på det här sättet innan. Jag kan ha fel och vara dålig på att googla, men jag hittar inget som liknar det här. Kan ju så klart bero på att det bara är vi nervösa svenskar som oroar oss över några ynka milliliter alkohol i maten.
Ett väldigt bra recept på rödvinssås httar ni här.